1ΓΔ―Γ‘ώΧβ Ά≠–Ω‘≠Βγ≥Ί(»γΆΦ)ΙΛΉς ±Θ§œ¬Ν––π ω’ΐ»ΖΒΡ «(ΓΓΓΓ)
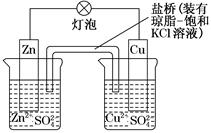
AΘ°’ΐΦΪΖ¥”ΠΈΣΘΚZn®DΓζZn2ΘΪΘΪ2eΘ≠
BΘ°Βγ≥ΊΖ¥”ΠΈΣΘΚZnΘΪCu2ΘΪ=Zn2ΘΪΘΪCu
CΘ°‘ΎΆβΒγ¬Ζ÷–Θ§ΒγΉ”¥”’ΐΦΪΝςœρΗΚΦΪ
DΘ°―Έ«≈÷–ΒΡKΘΪ“ΤœρZnSO4»ή“Κ
2ΓΔ―Γ‘ώΧβ “Μ―θΜ·ΒΣΚΆ“Μ―θΜ·ΧΦΕΦ «Τϊ≥ΒΈ≤ΤχάοΒΡ”–ΚΠΈο÷ Θ§ΥϋΟ«ΡήΜΚ¬ΐΒΊΖΔ…ζ»γœ¬Ζ¥”ΠΘΚ2NO(g)+2CO(g)  N2(g)+2CO2(g)(’ΐΖ¥”ΠΈΣΖ≈»»Ζ¥”Π)ΓΘœ÷άϊ”Ο¥ΥΖ¥”ΠΘ§Ρβ…ηΦΤ“Μ÷÷ΜΖ±ΘΉΑ÷Ο“‘Φθ«αΤϊ≥ΒΈ≤ΤχΕ‘¥σΤχΒΡΈέ»ΨΓΘœ¬Ν–…ηΦΤΖΫΑΗΩ…“‘ΧαΗΏΈ≤Τχ¥Πάμ–ßΙϊΒΡ «
N2(g)+2CO2(g)(’ΐΖ¥”ΠΈΣΖ≈»»Ζ¥”Π)ΓΘœ÷άϊ”Ο¥ΥΖ¥”ΠΘ§Ρβ…ηΦΤ“Μ÷÷ΜΖ±ΘΉΑ÷Ο“‘Φθ«αΤϊ≥ΒΈ≤ΤχΕ‘¥σΤχΒΡΈέ»ΨΓΘœ¬Ν–…ηΦΤΖΫΑΗΩ…“‘ΧαΗΏΈ≤Τχ¥Πάμ–ßΙϊΒΡ «
AΘ°≤ΜΕœœρΉΑ÷Ο÷–ΙΡ»κΩ’Τχ
BΘ°ΧαΗΏΖ¥”ΠΉΑ÷ΟΒΡΈ¬Ε»
CΘ°ΫΒΒΆΖ¥”ΠΉΑ÷ΟΒΡ―Ι«Ω
DΘ°‘ΎΖ¥”ΠΉΑ÷Ο÷–ΉΑ»κΦν ·Μ“
3ΓΔΧνΩ’Χβ 1200Γφ ±Ω…”ΟΖ¥”Π 2BBr3(g)+ 3H2(g)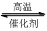 2B(s) + 6HBr(g) ά¥÷Τ»ΓΨßΧε≈πΓΘΆξ≥…œ¬Ν–ΧνΩ’ΘΚ
2B(s) + 6HBr(g) ά¥÷Τ»ΓΨßΧε≈πΓΘΆξ≥…œ¬Ν–ΧνΩ’ΘΚ
Θ®1Θ©œ¬Ν–ΥΒΖ®ΡήΥΒΟςΗΟΖ¥”Π¥οΒΫΤΫΚβΒΡ «______Θ®―ΓΧν–ρΚ≈Θ§œ¬Ά§Θ©ΓΘ
a. v’ΐ(BBr3)= 3vΡφ(HBr)? b. 2c(H2) = c(HBr)
c.Οή±’»ίΤςΡΎ―Ι«Ω≤Μ‘Ό±δΜ·? d. »ίΤςΡΎΤχΧεΤΫΨυΡΠΕϊ÷ ΝΩ≤Μ‘Ό±δΜ·
Θ®2Θ©»τΟή±’»ίΤςΧεΜΐ≤Μ±δΘ§…ΐΗΏΈ¬Ε»Θ§ΨßΧε≈πΒΡ÷ ΝΩ‘ωΦ”Θ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «_________ΓΘ
a. ‘ΎΤΫΚβ“ΤΕ· ±’ΐΖ¥”ΠΥΌ¬ œ»‘ω¥σΚσΦθ–Γ
b. ‘ΎΤΫΚβ“ΤΕ· ±ΡφΖ¥”ΠΥΌ¬ Φ÷’‘ω¥σ
c. ’ΐΖ¥”ΠΈΣΖ≈»»Ζ¥”Π
d. ¥οΒΫ–¬ΤΫΚβΚσΖ¥”ΠΈο≤Μ‘ΌΉΣΜ·ΈΣ…ζ≥…Έο
Θ®3Θ©»τ…œ ωΖ¥”Π‘Ύ10LΒΡΟή±’»ίΤςΡΎΖ¥”ΠΘ§5minΚσΘ§ΤχΧεΉή÷ ΝΩΦθ…Ό1.1 gΘ§‘ρΗΟ ±ΦδΕΈΡΎ«βΤχΒΡΤΫΨυΖ¥”ΠΥΌ¬ ΈΣ__________________ΓΘ
Θ®4Θ©Άυ»ίΤς÷–≥δ»κ0.2 mol BBr3ΚΆ“ΜΕ®ΝΩH2Θ§≥δΖ÷Ζ¥”Π¥οΒΫΤΫΚβΚσΘ§ΜλΚœΤχΧε÷–HBrΑΌΖ÷Κ§ΝΩ”κΤπ ΦΆ®»κH2ΒΡΈο÷ ΒΡΝΩ”–»γΆΦΙΊœΒΓΘ‘ΎaΓΔbΓΔc»ΐΒψ÷–Θ§H2 ΒΡΉΣΜ·¬ ΉνΗΏΒΡ «______Θ®―ΓΧνΉ÷ΡΗΘ©ΓΘbΒψ¥οΒΫΤΫΚβΚσΘ§‘Ό≥δ»κH2 ΙΤΫΚβΒΫ¥οcΒψΘ§¥ΥΙΐ≥Χ÷–ΤΫΚβ“ΤΕ·ΒΡΖΫœρΈΣ__________Θ®ΧνΓΑ’ΐœρΓ±ΓΔΓΑΡφœρΓ±ΜρΓΑ≤Μ“ΤΕ·Γ±Θ©ΓΘ
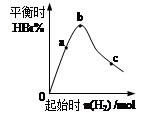
4ΓΔΦρ¥πΧβ ‘Ύ“ΜΟή±’ΒΡ1L»ίΤςάοΉΑ”–4mol?SO2ΚΆ2mol?O2Θ§‘Ύ“ΜΕ®ΧθΦΰœ¬ΩΣ ΦΖ¥”Π…ζ≥…SO3Θ°2m inΡ©≤βΒΟ»ίΤς÷–”–3.6mol?SO2Θ§ ‘ΦΤΥψΘΚ
Θ®1Θ©2minΡ©SO3ΒΡ≈®Ε»Θ°?Θ®2Θ©2minΡΎSO2ΒΡΤΫΨυΖ¥”ΠΥΌ¬ Θ°
Θ®3Θ©O2ΒΡΉΣΜ·¬ Θ°
5ΓΔΧνΩ’Χβ Θ®5Ζ÷Θ©‘ΎΟή±’»ίΤς÷–Θ§Β±Κœ≥…Α±ΒΡΖ¥”ΠN2+3H2===2NH3Θ®’ΐΖ¥”Π «Ζ≈»»Ζ¥”ΠΘ©¥οΒΫΤΫΚβ ±Θ§ΗΡ±δ»γœ¬ΒΡ“Μ–©ΧθΦΰΘΚ
AΘ°…ΐΈ¬Θ§
BΘ°Φ”―ΙΘ§
CΘ°Φθ―ΙΘ§
DΘ°‘ω¥σcΘ®H2Θ©Θ§Θ®EΘ©Φθ–ΓcΘ®NH3Θ©Θ§Θ®FΘ©‘ω¥σcΘ®NH3Θ©Θ§»τΤΫΚβœρ”““ΤΕ·”ΟΓΑ ΓζΓ±Θ§»τΤΫΚβœρΉσ“ΤΕ·”ΟΓΑΓϊΓ±±μ ΨΘΜ»τ÷Β‘ωΦ””ΟΓΑΓϋΓ±±μ ΨΘ§»τ÷ΒΦθ–Γ”ΟΓΑΓΐΓ±±μ ΨΘ§«κΗυΨίœ¬±μ÷–ΗςœνΒΡ±δΜ·«ιΩωΘ§‘ΎΗΡ±δΧθΦΰάΗΡΩ÷–Χν…œœύ”ΠΒΡ±ύΚ≈Θ®ΟΩœν÷ΜΗΡ±δ“ΜΗωΧθΦΰΘ©ΓΘ