1、选择题 已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是
A.原子半径: A>B>D>C
B.原子序数: d>c>b>a
C.离子半径: C>D>B>A
D.单质的还原性: A>B>D>C
参考答案:C
本题解析:aA2+、bB+、cC2-、dD-都具有相同的电子层结构,说明a、b的电子层比c、d的电子层数多,原子半径应该是B > A > C > D;原子序数是a>b>d>c;离子半径中C>D>B>A。单质的还原性应该是A>B>D>C。
点评:本题中微粒半径的比较中当电子层数相同时,核电荷数越高半径反而越小,而对于核电荷数相等的离子来说,电荷数越高,半径反而越小。
本题难度:简单
2、选择题 如果你在厨房不小心将花生油与凉开水混在一起,你将采用下列何种方法进行分离
A.过滤
B.蒸馏
C.分液
D.萃取
参考答案:C
本题解析:萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,分液适用于互不相溶的液体之间的一种分离方法,蒸馏是依据混合物中个组分沸点不同而分离的一种法,适用于除去易挥发、难挥发或不挥发杂质,过滤适用于不溶性固体和液体之间的一种分离方法。花生油不溶于水,分液即可,答案选C。
本题难度:困难
3、选择题 X、Y、Z、W是短周期元素,原子序数依次增大。X是原子半径最小的元素;Y元素原子的最外层电子数是电子层数的2倍;Z元素的-1价阴离子、W元素的+3价阳离子的核外电子排布均与氖原子相同。下列说法正确的是
A.X、Y形成的化合物只含有极性键
B.X单质和Z单质在暗处能剧烈反应
C.含W元素的盐溶液一定显酸性
D.Z离子半径小于W离子半径
参考答案:B
本题解析:X是原子半径最小的元素,为H元素;Y元素原子的最外层电子数是电子层数的2倍,为C元素;Z元素的-1价阴离子、W元素的+3价阳离子的核外电子排布均与氖原子相同,则Z为F元素、W为Al元素。A、X、Y形成的化合物为烃,可能含有非极性键,错误;B、H2与F2在暗处能剧烈反应,正确;D、具有相同电子排布的离子,原子序数越大,离子半径越小,所以离子半径:F?>Al3+,错误。
本题难度:一般
4、填空题 (9分)已知:A、B、C、D分别是中学化学中常见的四种不同粒子,它们之间有如下的反应关系:
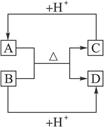
(1)如果A、B、C、D均是10电子粒子,请写出:A的化学式___________________。
(2)如果A和C是18电子的粒子,B和D是10电子粒子,请写出:
①A与B在溶液中反应的离子方程式:___________________________________________。
②根据上述离子方程式,可以判断C与B结合质子的能力大小是(用化学式或离子符号表示):___________________>___________________。
参考答案:(1) 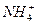 ?
?
(2)① H2S + 2OH-====S2-+2H2O
②OH-? S2-
本题解析:常见的10电子粒子有:CH4、NH3、H2O、HF、OH-、H3O+、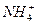 等。常见的18电子粒子有:H2S、HCl、S2-、Cl-、K+、Ca2+等。
等。常见的18电子粒子有:H2S、HCl、S2-、Cl-、K+、Ca2+等。
本题难度:简单
5、填空题 已知有五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物A2B中所有的离子的电子数都相同,其电子总数为30;D和E可形成4核10电子分子。试回答下列问题:
1. 写出下列元素的名称:A?,B?
2. 写出D元素的原子结构示意图?,C元素在周期表中的位置?。
3. 写出下列物质的电子式
E与B形成的化合物:?
A、B、E形成的化合物:?
D、E形成的化合物:?
4. 写出C的最高价氧化物对应水化物的浓溶液与铜反应的化学方程式?
写出D的最高价氧化物对应水化物的稀溶液与铜反应的离子方程式?
参考答案:(本题共11分,前3小题每个问题各1分,第4小题各个方程式2分)
1、A?钠?,B?氧? 2、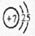 ?,第三周期ⅥA族
?,第三周期ⅥA族
3、 (?或
(?或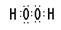 )?、?
)?、?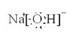 ?、?
?、? ?
?
4、 、
、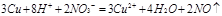
(不注明浓、不写明条件、不配平均不给分)
本题解析:(1)A与B形成的离子化合物A2B中所有的离子的电子数都相同,其电子总数为30,所以A是Na,B是O。又因为原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族,所以C是S。D和E可形成4核10电子分子,因此D是N,E是H。
(2)氮元素的原子序数是7,其原子结构示意图为 ;S的原子序数是16,位于第三周期ⅥA族。
;S的原子序数是16,位于第三周期ⅥA族。
(3)H和O可以形成水和双氧水,都是共价化合物,其电子式分别是 、
、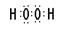 ;A、B、E形成的化合物是氢氧化钠,含有离子键和极性键,电子式是
;A、B、E形成的化合物是氢氧化钠,含有离子键和极性键,电子式是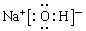 ;D、E形成的化合物是氨气,含有极性键,电子式是
;D、E形成的化合物是氨气,含有极性键,电子式是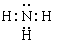 。
。
(4)C的最高价氧化物对应水化物是硫酸,浓硫酸具有氧化性,和铜反应的方程式是2H2SO4(浓)+Cu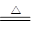 CuSO4+2H2O+SO2↑;D的最高价氧化物对应水化物是硝酸,硝酸也具有氧化性,和铜反应的离子方程式是3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑。
CuSO4+2H2O+SO2↑;D的最高价氧化物对应水化物是硝酸,硝酸也具有氧化性,和铜反应的离子方程式是3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑。
点评:本题属于位、构、性的综合考查,需要熟练掌握元素周期表的结构,然后结合已知的条件逐一推断即可。
本题难度:一般