1��ѡ���� ���ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ����±���
Ԫ�ش���
| L
| M
| Q
| R
| T
|
ԭ�Ӱ뾶/nm
| 0.160
| 0.143
| 0.104
| 0.111
| 0.066
|
��Ҫ���ϼ�
| +2
| +3
| +6��-2
| +2
| -2
|
����������ȷ����
A��R��M�ĵ��ʼ��仯���������ƵĻ�ѧ����
B��L��M�ĵ��ʾ��õ�������ڵ��εķ���ұ������
C��T���⻯�ﻹԭ�Լ��ȶ��Ծ���Q���⻯��ǿ
D������Ԫ�صij����������а뾶������Q2��
�ο��𰸣�AD
����������ɸ�Ԫ�ص���Ҫ���ϼۼ�ԭ�Ӱ뾶���ɿ�֪��L��RΪ��IIAԪ�أ��ֱ�ΪMg��Be��Q��TΪ��VIAԪ�أ��ֱ�ΪS��O����MΪ��Ԫ��
A����Ԫ����ѭ�Խ��߹����������ƣ���ȷ
B��������ڵ��Ȼ�þ��ȡþ����ұ�����ǵ�����ڵ�������������ȷ
C��O�ķǽ����Խ�Sǿ�����⻯����ȶ��Խ�ǿ������ԭ�Խ���������ȷ
D�������ӵĵ��Ӳ������ľ��������ӣ���ȷ
��ΪAD
�����Ѷȣ�һ��
2������� ��13�֣����ִ�ս���У�����̹��ս����õ�װ�ײ����Ǿ������ƺ��ȴ�����ĺϽ�֣��ȴ���������װ�ṹ�Ļ�ѧ�ͻ�е���Ժ�����ȵı���һ�¡����кϽ�Ԫ�صİٷֱȺ���Ϊ����0.5~1.25?��0.5~1.5 ��0.3~0.6?��0.8~1.6?̼0.3
��1����Ԫ�صĻ�̬ԭ�ӵļ۵��Ӳ��Ų�ʽ��?��
��2��CԪ������ͬ������һ����Ԫ����ɵľ����У�Cԭ�ӵ��ӻ���ʽΪ��������.
��3��Mn��Fe�IJ��ֵ��������������
Ԫ?��
| Mn
| Fe
|
������
/kJ��mol��1
| I1
| 717
| 759
|
I2
| 1509
| 1561
|
I3
| 3248
| 2957
|
?
���ݱ����ݣ���̬Mn2����ʧȥһ�����ӱ���̬Fe2����ʧȥһ�������ѣ���ԭ����?��
��4������Ni�����γɶ��������Ҹ���������й㷺����;��
ij�������ṹ����ͼ��ʾ�������ں��е�������
��?������ţ���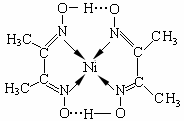
A�����? B�����Ӽ�? C�����ۼ�? D��������? E����λ��
��ɸ�����������ͬ���ڶ�����Ԫ�صĵ縺���ɴ�С��˳����?����?��
��5������������CO�����������ȣ�������ɫ�ӷ���Һ̬Ni(CO)4���������幹�͡�423Kʱ��Ni(CO)4�ֽ�ΪNi��CO���Ӷ��Ƶøߴ��ȵ�Ni�ۡ����Ʋ⣺���ʻ����ľ���������?����?
��6�������뵪�γ�һ�ִ��Բ��ϣ��侧���ṹ����ͼ��ʾ����ô��Բ��ϵĻ�ѧʽΪ ?
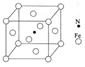
�ο��𰸣���1��3d54S1?��2��?sp3?
��3��Mn2��ת��ΪMn3��ʱ��3d�ܼ��ɽ��ȶ���3d5�����״̬ת��Ϊ���ȶ���3d4״̬����Fe2��ת��ΪFe3��ʱ��3d�ܼ��ɲ��ȶ���3d6״̬ת��Ϊ���ȶ���3d5�����״̬����
��4�� ACE; ?N��O��C��?��5�� ���Ӿ���?��6��Fe4N
�����������1��ԭ�Ӵ���ȫ�������������ȫ��ʱ���ȶ���״̬��24�Ÿ�Ԫ�صĻ�̬ԭ�ӵļ۵����Ų�ʽ��3d54S1����2��CԪ��SiԪ����ɵ�SiC������ԭ�Ӿ��塣���е�Cԭ�ӵ��ӻ���ʽΪsp3����3�����ݱ����ݣ���̬Mn2����ʧȥһ�����ӱ���̬Fe2����ʧȥһ�������ѣ���ԭ����Mn2��ת��ΪMn3��ʱ��3d�ܼ��ɽ��ȶ���3d5�����״̬ת��Ϊ���ȶ���3d4״̬����Fe2��ת��ΪFe3��ʱ��3d�ܼ��ɲ��ȶ���3d6״̬ת��Ϊ���ȶ���3d5�����״̬������4����ij��������к��й��ۼ�����λ���������ѡ��ΪACE����ɸ�����������ͬ���ڶ�����Ԫ����C��N��O��һ������£�Ԫ�صķǽ�����Խǿ��ԭ�Ӱ뾶ԽС��Ԫ�صĵ縺�Ծ�Խ���Ƕ���Nԭ����˵���������������Ӵ��ڰ�������ȶ�״̬������ʧȥ������Ҫ��������O���ࡣ���������Ԫ�صĵ縺���ɴ�С��˳����N��O��C����5�� �������ʻ��������ʿ���֪�þ������Է��Ӿ��塣��6��Fe��8��1/8+6��1/2=4��N��1����˸ô��Բ��ϵĻ�ѧʽΪFe4N��
�����Ѷȣ�һ��
3��ѡ���� X��Y��Z��ΪԪ�����ڱ���ǰ20��Ԫ�أ�mXa+��nYb����Z��b+1���������ӵĵ��Ӳ�ṹ��ͬ������˵����ȷ����?��?��
A����֪mXa+��nYb������m+a=n��b
B�����Ӱ뾶��Yb��>Z��b+1������Xa+
C��Z(b+1)���Ļ�ԭ��һ������Yb��
D����̬�⻯����ȶ���Hb+1Zһ������HbY
�ο��𰸣�C
���������mXa+��nYb����Z��b+1�������ӵĵ��Ӳ�ṹ��ͬ��������������ͬ����m-a=n+b��X����Y��Z����һ���ڣ�XΪ����Ԫ�أ�Y��ZΪ�ǽ���Ԫ�أ�X��ԭ����������Y��ԭ��������Y��ԭ����������Z��ԭ����������ϵ��Ӳ�ṹ��ͬ�˵����Խ�����Ӱ뾶ԽС��Ԫ���������жϡ�
A���������������m-a=n+b���ʴ���B����е��Ӳ�ṹ��ͬ�����ӣ��˵����Խ��뾶ԽС���ʴ���D�Y�ķǽ����Դ���Z�ķǽ����ԣ��ʴ�����ѡC��
���������⿼���˰뾶�Ƚϡ���������Ų����ṹ��λ�ù�ϵ���ѶȲ����ж�W��Y��λ�ù�ϵ�ǹؼ���Ҫ�������Ԫ��������֪ʶ���
�����Ѷȣ���
4������� (13��)��ͼ��Ԫ�����ڱ���һ���֣����еĢ١�����Ԫ�أ�����ѧ������ջش�
��
����
| I A
| IIA
| IIIA
| ��A
| VA
| ��A
| ��A
| 0
|
��
| ?
| ?
| ?
| ��
| ��
| ?
| ��
| ?
|
��
| ?
| ��
| ��
| ��
| ?
| ?
| ��
| ��
|
��
| ��
| ?
| ?
| ?
| ?
| ?
| ��
| ?
|
?
��1������ЩԪ���У���ԭ�ӵ�ԭ�ӽṹʾ��ͼΪ?��
��2��д���ٵ����������͢ڵĵ��ʵĵ���ʽ?��?��
��3���õ���ʽ��ʾ������γɻ�����Ĺ���?��
��4���ٵĵ��ʺ͢������ﷴӦ�Ļ�ѧ����ʽ?��
��5��д���ݵĵ������������Ʒ�Ӧ�Ļ�ѧ����ʽ��??
д���ݵ���������������������Һ��Ӧ�����ӷ���ʽ��??��
��6����֪��l mol C��H����l mol O=O����l molC=O����l mol H��O���ֱ���Ҫ���յ�����Ϊ414kJ��498kJ��728kJ��464kJ����l mol������ȫȼ�շų�?kJ��������
�ο��𰸣���1��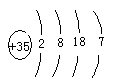
��2��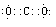
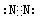
��3��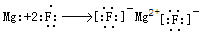
��4��2C+SiO2 ?Si+2CO��;
?Si+2CO��;
��5��2Al+2H2O +NaOH=2NaAlO2+3H2��;Al(OH)3+OH-=AlO-2+2H2O��
��6��660
�����������1����ԭ����Brԭ�ӣ�������35�����ӣ�ԭ�ӽṹʾ��ͼΪ ��
��
��2���ٵ������������CO2������ʽΪ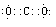 ���ڵĵ�����N2������ʽΪ
���ڵĵ�����N2������ʽΪ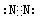 ��
��
��3��������γɻ�������MgF2���������ӻ����Mgʧȥ2�����ӳ�Ϊþ���ӣ�F�õ�1�����ӳ�Ϊ�����ӣ��õ���ʽ��ʾ���γɹ�����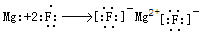 ��
��
��4���ٵĵ��ʺ͢������ﷴӦ��C�������������·����û���Ӧ����ѧ����ʽΪ2C+SiO2 ?Si+2CO��;
?Si+2CO��;
��5������Al�����������Ʒ�Ӧ�Ļ�ѧ����ʽΪ2Al+2H2O +NaOH=2NaAlO2+3H2��;�����������������д���ӷ���ʽʱ���ܲ�������������������������Һ��Ӧ�����ӷ���ʽΪAl(OH)3+OH-=AlO-2+2H2O��
��6������������ȼ�յĻ�ѧ����ʽΪCH4+2O2 CO2+ 2H2O�����ݷ�Ӧ���뻯ѧ�����ܵĹ�ϵ����H=��4��414+2��498-2��728-2��2��464��kJ/mol="-660" kJ/mol������1mol������ȫȼ�շų�660kJ��������
CO2+ 2H2O�����ݷ�Ӧ���뻯ѧ�����ܵĹ�ϵ����H=��4��414+2��498-2��728-2��2��464��kJ/mol="-660" kJ/mol������1mol������ȫȼ�շų�660kJ��������
�����Ѷȣ�һ��
5��ѡ���� ���й���ԭ�ӽṹ��Ԫ�����ʵ�˵����ȷ����(�� ��)��
A��������ǽ�����ɵĻ�������ֻ�����Ӽ�
B����A���Ԫ����VIIA��Ԫ���γɵĻ����ﲻһ�������ӻ����
C����ͬԭ����ɵĴ�����һ���ǻ����
D����A ��Ԫ�ص�������������Խǿ,������������Ӧˮ����ļ���Խǿ
�ο��𰸣�B
���������������ǽ�����ɻ�������ܲ������Ӽ����磺 AlCl3�ȣ�Ҳ�����ں����Ӽ�ʱ���й��ۼ�����: NaOH�ȣ�A������A���Ԫ����H�ͼ������������±�ؿ����γɹ��ۼ���Ҳ���γ����Ӽ����磺HCl��NaCl�ȣ�B�ԡ�C�в�ͬԭ�Ӳ�һ���Dz�ͬԪ�أ��磺뭡�뮡���Dz�ͬԭ�ӣ���������Ԫ�أ�HDҲ�������ǵ��ʡ���ͬһ�������������������Խǿ��Ԫ�صĽ�����Խ����������������Ӧˮ�������Խ����D����
�����Ѷȣ�һ��