|
|
|
高考化学知识点总结《原电池原理》高频试题强化练习(2019年最新版)(一)
2020-07-08 01:40:43
【 大 中 小】
|
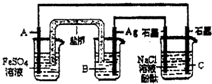
1、选择题 利用反应:2Ag(aq)+Fe(s)=Fe2+(aq)+2Ag(s)设计原电池并用它作电源进行电解的装置如图所示.NaCl溶液的体积为200mL,假设反应产生的气体全部放出,且反应前后溶液体积的变化忽略不计.下列有关叙述错误的是( )
A.电极A应该用Fe作材料,B是AgNO3溶液,电极C周围溶液变红
B.A、C两极都发生氧化反应,C电极反应式为:2H++2e-=H2↑
C.银电极变粗,为电源的正极,A电极反应式为:Fe-2e-=Fe2+
D.当析出Ag21.6g时,NaCl溶液的pH是反应前的2倍
| 
2、填空题 铝与镁在不同的电解质溶液中分别组成原电池A,B。
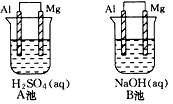
(1)指出各池中的负极材料并写出其电极反应式_________________________。
(2)从构成原电池的几个组成部分来看,判断原电池负极,除了要考虑金属的活动性外,还要考虑
____________________。
3、填空题 (9分)(1)X、Y、Z、W四种金属片进入稀盐酸中,用导线连接,可以组成原电池,实验结果如下图所示,则四种金属的活泼性由强到弱的顺序为______ _____
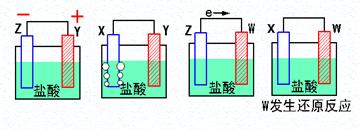
(2)假设第一个装置中两个金属片一个是铝片一个是铜片,电解质溶液是盐酸,请写出两极的电极反应式:正极 、负极
(3)用KOH溶液做电解质溶液的氢氧燃料电池的正极反应式
4、选择题 如图是模拟电化学反应装置图。下列说法正确的是(?)

A.开关K置于N处,则铁电极的电极反应式为:Fe-2e-=Fe2+
B.开关K置于N处,可以减缓铁的腐蚀
C.开关K置于M处,则铁电极的电极反应式为:2Cl--2e-=Cl2↑
D.开关K置于M处,电子从碳棒经开关K流向铁棒
5、选择题 下列关于实验现象的描述不正确的是
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用铜片做阳极,铁片做做阴极,电解氯化铜溶液,铁片表面出现一层铜
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
|
