1、选择题 每年4到10月份,尤其是夏季7、8月份,随着气温的上升,宁波大气首要污染物多为臭氧,下列有关臭氧的叙述不正确的是
A.要尽量避免在阳光照射强烈(温度越高,臭氧浓度较高)的中午前后外出
B.复印机在工作过程中会使周围空气产生臭氧,要尽量避免长时间待在复印室
C.臭氧层能使地球上的生物免受太阳光中紫外线的伤害
D.臭氧可用于净化空气、饮用水,杀菌消毒;使用时,臭氧浓度越大越好
参考答案:D
本题解析:分析:大气中的臭氧层可吸收紫外线,对地球起保护作用,但臭氧具有强氧化性,少量臭氧(O3)可以起到消毒、杀菌作用,但臭氧过量对人体有害.
解答:A.臭氧具有强氧化性,臭氧过量对人体有害,所以要尽量避免在阳光照射强烈(温度越高,臭氧浓度较高)的中午前后外出,故A正确;
B.臭氧具有强氧化性,臭氧过量对人体有害,所以要尽量避免长时间待在复印室,故B正确;
C.大气中的臭氧层可吸收紫外线,对地球上生物起保护作用,免受紫外线的照射,故C正确;
D.臭氧具有强氧化性,所以能杀菌消毒,但臭氧过量对人体有害,故D错误;
故选D.
点评:本题考查臭氧的性质,知道臭氧性质的利弊,合理运用臭氧,使其服务于人类.
本题难度:一般
2、选择题 在下列气体的制取中,均用到浓硫酸。浓硫酸只起脱水剂作用的是()
A.浓硫酸与甲酸加热制取CO
B.浓硫酸与铜反应制取SO2
C.浓硫酸与无水乙醇反应制取乙烯
D.浓硫酸与亚硫酸钠反应制取SO2
参考答案:A
本题解析:浓硫酸与甲酸反应制CO,浓硫酸只起脱水剂作用,A正确;浓硫酸与铜反应,浓硫酸起氧化剂和酸的作用;与无水乙醇反应制乙烯,浓硫酸起催化剂和脱水剂作用;与Na2SO3反应制SO2,浓硫酸只起酸的作用。
本题难度:简单
3、选择题 下列离子方程式中,正确的是(?)
A.金属钠与冷水反应:Na+2H2O====Na++2OH-+H2↑
B.碳酸钙投入醋酸溶液中CaCO3+2CH3COOH====Ca2++2CH3COO-+H2O+CO2↑
C.向Ca(ClO)2溶液中通过量CO2气体:Ca2++2ClO-+CO2+H2O====CaCO3↓+2HClO
D.向硫酸铜溶液中滴入Ba(OH)2溶液:Ba2++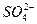 ====BaSO4↓
====BaSO4↓
参考答案:B
本题解析:A项中离子方程式没有配平;C项中应该生成Ca(HCO3)2,而不是CaCO3;D项中离子方程式应该是:Cu2++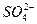 +Ba2++2OH-====Cu(OH)2↓+BaSO4↓。所以B正确。
+Ba2++2OH-====Cu(OH)2↓+BaSO4↓。所以B正确。
本题难度:简单
4、选择题 下列关于浓硝酸和浓硫酸的叙述正确的是(?)
A.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
B.浓硝酸具有不稳定性,实验室里应保存在棕色瓶中
C.常温下,浓硝酸可以跟铜缓慢反应,浓硫酸可与铜片迅速反应
D.实验室可以用浓硝酸来制氢气
参考答案:B
本题解析:氨气是碱性气体,不能用浓硫酸来干燥,用碱石灰干燥氨气。常温下铜和浓硫酸不反应,在加热时才能反应。硝酸是氧化性酸和金属反应不能生成氢气。答案选B。
本题难度:一般
5、计算题 臭氧能与KI溶液反应,生成一种可使带余烬的木条复燃的气体,向反应后溶液中滴入酚酞变成红色,若滴入淀粉溶液则变成蓝色。为测定大气中臭氧的含量,将0℃,1.01×105Pa,33.6m3的空气通过KI溶液,使之完全反应,在所得溶液中用0.01mol/L的Na2S2O3溶液60mL恰好与之反应完全(反应式为</PGN0047A.TXT/PGN>2Na2S2O3+I2=Na2S4O6+2NaI)。
(1)完成下列方程式:O3+KI+H2O→____
(2)计算大气中臭氧的体积分数。
参考答案:(1)O3+2KI+H2O=O2+I2+2KOH
(2)空气中含臭氧的体积为2×10-5%
本题解析:(1)O3+2KI+H2O=O2+I2+2KOH
(2)设空气中含臭氧的体积为x
依题意:O3~I2~2Na2S2O3
22.4L?2 mol
X? 0.01 mol/L×0.060L
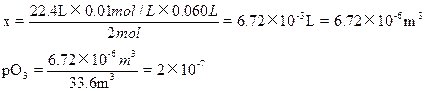
本题难度:一般