1、选择题 在下列气体的制取中,均用到浓硫酸。浓硫酸只起脱水剂作用的是()
A.浓硫酸与甲酸加热制取CO
B.浓硫酸与铜反应制取SO2
C.浓硫酸与无水乙醇反应制取乙烯
D.浓硫酸与亚硫酸钠反应制取SO2
2、实验题 (16分)某研究性学习小组为研究铁粉与浓硫酸反应所生成气体的成份并测定各气体的含量,进行了如下实验:
【实验推测】足量的铁粉与浓硫酸反应能生成SO2和H2两种气体。
(1)该小组作出此推测的理由是:?。
【实验准备】a.供选择的药品:铁粉、浓硫酸、氧化铜粉末、0.2 mol/L的H2C2O4标准溶液、0.1 mol/L的酸性KMnO4标准溶液、酸碱指示剂。
b.实验装置设计及组装(加热及夹持装置均已略去)
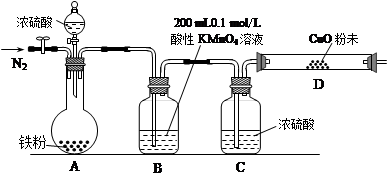
【实验过程及数据处理】
(2)B中发生反应的离子方程式为:?。
(3)实验前先通入一段时间的N2,其目的是?。
(4)B、C、D中所盛试剂均足量,则证实生成的气体中同时存在SO2和H2的现象是?
?。
(5)A中反应结束后,继续通N2使A中生成的气体全部赶出,待B、D中反应完全后,先后三次取用B中反应后的溶液于锥形瓶中,每次取用25 mL,用H2C2O4标准溶液进行滴定。
①H2C2O4标准溶液与酸性KMnO4溶液反应的离子方程式如下,请将该方程式完成并配平。
(? )H2C2O4+(? )MnO4- +(? )H+ =(? )Mn2+ +(? ) H2O+(? ) (? )
②滴定达到终点时的现象是?。
③重复滴定两次,平均每次耗用H2C2O4标准溶液15.63 mL,则铁与浓硫酸反应产生的SO2气体的物质的量为?;经称量,实验前后装置D的质量减少0.9 g,则产生的气体中SO2的体积分数为?。
3、选择题 下列气体不能用浓硫酸作干燥剂的是(?)
①HCl?②NH3?③Cl2?④H2?⑤SO2?⑥SO3
A.①②⑥
B.②⑤⑥
C.①⑥
D.②⑥
4、选择题 下列反应生成的新化合物中,不稳定的是?(?)
A.SO3与水
B.SO2与水
C.SO2与氯水
D.SO3与NaOH溶液
5、选择题 在硫酸的工业制法中,下列对生产操作与生产操作的主要原因的说明都正确的是()
A.硫铁矿燃烧前需要粉碎,因为大块的硫铁矿不能燃烧
B.从沸腾炉出来的炉气需要净化,因为炉气中SO2会与杂质反应
C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
D.用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全