微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分)阅读下列材料后回答问题:一个体重50Kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
(1)在人体中进行Fe2+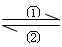 Fe3+的转化时,实现①的转化需消耗 剂(填氧化或还原),
Fe3+的转化时,实现①的转化需消耗 剂(填氧化或还原),
通常用 (填试剂名称)检验Fe3+存在。
(2)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作 剂,Fe3+发生 反应。
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的离子方程式为 。
参考答案:(1)氧化 硫氰酸钾; &#
本题解析:
试题解析:(1)①过程Fe2+失电子生成Fe3+,故Fe2+作还原剂,需要消耗氧化剂实现①,通常检验Fe3+存在的试剂为硫氰酸钾;(2)由题意知,Fe3+是氧化剂,维生素C是还原剂,Fe3+发生还原反应;(3)胃酸的主要成分是盐酸,铁与盐酸反应生成氯化亚铁和氢气,离子方程式为:Fe+2H+==Fe2++H2↑。
考点:氧化性、还原性强弱的比较
本题难度:一般
2、选择题 下列反应的离子方程式错误的是
A.碳酸钙跟盐酸反应: CaCO3+2H+→Ca2+ + CO2↑+H2O
B.铁跟氯化铜溶液反应:Fe + Cu2+→ Cu + Fe2+
C.氯化铵水解:NH4+ + H2O NH3?H2O+ H+
NH3?H2O+ H+
D.氢氧化钡溶液跟稀硫酸反应: Ba2+ + OH- + H+ + SO42-→ BaSO4↓+ H2O
参考答案:D
本题解析:氢氧化钡溶液跟稀硫酸反应: Ba2+ + 2OH- +2 H+ + SO42-→ BaSO4↓+2 H2O
本题难度:一般
3、选择题 下列离子方程式正确的是
A.向氨水中滴入盐酸:OH- + H+ =H2O
B.氢氧化钡溶液与稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O
C.铜粉溶于FeCl3溶液中:Cu+Fe 3+=" Fe" 2+ + Cu2+
D.Cl2与冷NaOH溶液反应:Cl2+2OH-= Cl-+ClO-+ H2O
参考答案:D
本题解析:
正确的为D
A.向氨水中滴入盐酸:NH3・H2O + H+ =H2O+NH4+
B.氢氧化钡溶液与稀硫酸:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
C.铜粉溶于FeCl3溶液中:Cu+2Fe 3+="2" Fe 2+ + Cu2+
D.正确
本题难度:一般
4、填空题 为证明Fe3+具有较强的氧化性,甲同学做了如下实验:将Cu片放入0.5mol/L Fe(NO3)3溶液中,观察到Cu片逐渐溶解,溶液由黄色变为蓝绿色,由此甲同学得到Fe3+具有较强氧化性的结论。
乙同学提出了不同的看法:“Fe(NO3)3溶液具有酸性,在此酸性条件下NO3-也能氧化Cu”,并设计实验进行探究。已知:
水解反应
| 平衡常数(K)
|
Fe3+ + 3H2O  Fe(OH)3 + 3H+ Fe(OH)3 + 3H+
| 7.9 × 10-4
|
Fe2+ + 2H2O  Fe(OH)2 + 2H+ Fe(OH)2 + 2H+
| 3.2 × 10-10
|
Cu2+ + 2H2O  Cu(OH)2 + 2H+ Cu(OH)2 + 2H+
| 3.2 × 10-7
请回答:(1)稀硝酸和Cu反应的化学方程式为 。
(2)请利用所提供的试剂,帮助乙同学完成实验方案设计。
试剂:0.5mol/L Fe(NO3)3溶液、Cu片、精密pH试纸(0.5~5.0)、硝酸钠溶液、稀盐酸。
方案: 。
(3)丙同学分别实施了甲、乙两位同学的实验方案,并在实验过程中用pH计监测溶液pH的变化,实验记录如下。
|