微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式中,正确的是
A.稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑
B.碳酸氢钠溶液与稀盐酸混合:HCO3-+H+=H2O+CO2↑
C.硫酸铜溶液与氢氧化钠溶液混合:CuS04+20H-=Cu(OH)2↓+SO42-
D.硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-=AgCl↓+N03-
2、填空题 为证明Fe3+具有较强的氧化性,甲同学做了如下实验:将Cu片放入0.5mol/L Fe(NO3)3溶液中,观察到Cu片逐渐溶解,溶液由黄色变为蓝绿色,由此甲同学得到Fe3+具有较强氧化性的结论。
乙同学提出了不同的看法:“Fe(NO3)3溶液具有酸性,在此酸性条件下NO3-也能氧化Cu”,并设计实验进行探究。已知:
水解反应
| 平衡常数(K)
|
Fe3+ + 3H2O  Fe(OH)3 + 3H+ Fe(OH)3 + 3H+
| 7.9 × 10-4
|
Fe2+ + 2H2O  Fe(OH)2 + 2H+ Fe(OH)2 + 2H+
| 3.2 × 10-10
|
Cu2+ + 2H2O  Cu(OH)2 + 2H+ Cu(OH)2 + 2H+
| 3.2 × 10-7
请回答:(1)稀硝酸和Cu反应的化学方程式为 。
(2)请利用所提供的试剂,帮助乙同学完成实验方案设计。
试剂:0.5mol/L Fe(NO3)3溶液、Cu片、精密pH试纸(0.5~5.0)、硝酸钠溶液、稀盐酸。
方案: 。
(3)丙同学分别实施了甲、乙两位同学的实验方案,并在实验过程中用pH计监测溶液pH的变化,实验记录如下。
实验内容
| 实验现象
| 甲同学的实验方案
| 溶液逐渐变成蓝绿色, pH略有上升
| 乙同学的实验方案
| 无明显现象,pH没有明显变化。
①据实验现象写出发生反应的离子方程式: 。
②导致实验过程中溶液pH略有上升的可能原因是 。
③解释乙同学的实验现象 。
(4)请你设计更简便可行的实验方案,帮助甲同学达到实验目的: 。
3、简答题 (10分)(1)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液中,设由水电离产生的OH-的物质的量浓度分别为A和B,则A________B(填“>”、“=”或“<”)。
(2)在纯碱溶液中滴入酚酞,溶液变红色,若向该溶液中再滴入过量的BaCl2溶液,所观察到的现象是_________________________,其原因是_________________________。
(3)对于盐AmBn的溶液:①若为强酸弱碱盐,其水解的离子方程式是_______________。
②若为弱酸强碱盐,其第一步水解的离子方程式是___________________________。
4、选择题 下列离子方程式书写正确的是
A.硫酸镁溶液跟氢氧化钡溶液反应: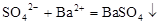
B.NaHCO3溶液与NaOH溶液反应:OH
5、填空题 (12分)写出下列反应的离子方程式
(1)过氧化钠与水
(2)金属铝与稀硫酸溶液
(3)向Na2CO3与NaHCO3混和溶液加入CaCl2溶液
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示有关生成H2的变化:
(A)
(B)
(5)把铜片放入稀硝酸中: ;
|
|